硫酸亚铁_硫酸亚铁简介
以工业废弃物硫酸亚铁为原料,加入碳酸氢铵和氯化钾,通过一系列化学反应和过滤、蒸发、煅烧等步骤,可制得硫酸钾、氯化铵、氧化铁红和液态二氧化碳。原料中各主要成分的利用率均达94%以上。“建业净水”
硫酸亚铁通常带有7个结晶水,分子式为FeSO4.7H2O,又称绿矾。其主要来源有二种:
(1)钛白生产中的副产物。用硫酸法生产钛白时,每制1t钛白粉副产4.5~5.0t绿矾。全国每年约副产75万t绿矾。除少量用于生产氧化铁红、饲料添加剂、水处理剂外,绝大部分作为废料弃去。
(2)从钢铁浸洗液中回收。钢材加工时常常需要用硫酸浸洗,我国每年可从浸洗液中回收绿矾约15万t,绝大部分未利用。
大量利用硫酸亚铁的方法有二种:一是按一定比例混入硫铁矿中用于制硫酸[1];二是用于制硫酸钾。由于硫酸钾属优质无氯肥料,需求量较大,因此是更有发展前途的利用方法。自70年代以来,发表了不少有关用硫酸亚铁制硫酸钾的专利文献[2~6],但迄今为止尚未见工业化的报道。
本研究以绿矾、碳酸氢铵和氯化钾为原料制备硫酸钾,同时副产氯化铵、氧化铁红和液态二氧化碳。这种方法使原料得到综合利用,既可解决绿矾的污染问题,又可产生较好的经济效益。据文献检索,至今尚未发现有类似的工艺。
绿矾的综合利用主要根据以下3个反应:
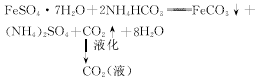 (1)
(1)
![]() (2)
(2)
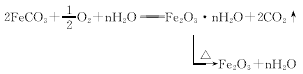 (3)
(3)
由于FeCO3的溶度积很小(Ksp=3.2×10-11),因此反应(1)可视为不可逆反应。该反应包括气液固三相传质过程,CO2气体的逸出造成液固表面滞流膜的不断更新,使传质阻力大大减小,FeSO4和NH4HCO3的溶解速度和反应速率增大,所以FeCO3生成速率很大,生成的固体粒子粒径很小。反应释放的CO2气体纯度高,可用于制液体CO2,也可用NaOH或KOH溶液吸收制食用小苏打或碳酸钾产品。
反应(2)为可逆反应,K2SO4产率由K+,NH+4‖Cl-,SO2-4——H2O四元体系溶解度图所决定。在20~40℃的温度范围内,K2SO4的最大产率为80%左右[7],实际产率仅60%~70%。本研究采用添加有机溶剂降低K2SO4在上述体系中溶解度的方法,使K2SO4的实际产率提高到85%以上。
FeCO3氧化为Fe2O3.2H2O的反应为不可逆反应,也属气液固三相反应。常温下反应速度较慢,温度提高反应速度加快。但反应速度过快,易造成氧化不完全,有少量Fe3O4生成,影响氧化铁红颜色。
根据反应原理拟定的绿矾综合利用工艺流程如图1所示。该工艺由5部分组成:
|
(1)FeSO4.7H2O和NH4HCO3反应,制(NH4)2SO4溶液、FeCO3固体和CO2气体; 本信息来自》巩义市建业净水材料有限公司》http://www.gyjyjs.net 销售文章推荐》活性炭按来源、制造方法、外观形状等细分水处理活性炭
|